
지난 포스팅까지 열역학 제 1법칙, 2법칙과 그 의미, 다양한 서술 등에 대해 자세히 알아보았다. 오늘 포스팅에서는, 열역학 제 2법칙에서 대단히 중요한 개념인 카르노 기관에 대해 알아보고, 그 의미와 엔트로피에 대해 알아보도록 하겠다.
열역할 제 2법칙과 관련해서는 아래 포스팅들에 세세히 정리놓았으니 한 번 읽어보기를 권장한다. 지금까지의 열역학 포스팅들을 쭉 읽어보는 것도 좋을 것 같다.
[열역학] 1.5 자발, 비가역성과 엔트로피, 클라우지우스 부등식-(Spontaneous, Irreversibility and Entropy, In
[열역학] 1.5 자발적 과정과 비가역적 과정, 비가역성과 엔트로피, 클라우지우스 부등식-Spontaneous and Irreversible Process, Irreversibility and Entropy, Inequality of Clausius 지난 포스팅까지는 열역학 제 1법칙에
gyuuuul.tistory.com
2025.09.11 - [전공 공부정리/열역학] - [열역학] 1.6 열역학 제 2법칙 - 정의, 클라우지우스 서술과 켈빈-플랑크 서술, 열역학 제 1법칙과의 결합
[열역학] 1.6 열역학 제 2법칙 - 정의, 클라우지우스 서술과 켈빈-플랑크 서술, 열역학 제 1법칙과
[열역학] 1.6 열역학 제 2법칙 - 정의, 클라우지우스 서술과 켈빈-플랑크 서술, 열역학 제 1법칙과의 결합 지난 포스팅에서는 열역학적인 자발과 비가역성에 대해 그 의미를 알아보고, 이와 관련된
gyuuuul.tistory.com
2025.09.17 - [전공 공부정리/열역학] - [열역학] 1.7 열역학 제 2법칙 - 등온과정, 단열과정, 자유팽창
[열역학] 1.7 열역학 제 2법칙 - 등온과정, 단열과정, 자유팽창
지난 포스팅까지 열역학 제 1법칙과 2 법칙과 그 의미, 다양한 서술 등에 대해 자세히 알아보았다. 열역학에서는 특히 열역학적 과정(등온, 단열, 등적, 등압 등등)을 정확히 이해하는 것이 매우
gyuuuul.tistory.com
그럼 시작해보자~~!!
1. 열기관(Heat Engine)
열기관은 열에너지를 역학적 에너지로 변환해주는 장치다. 근본적으로 두 개의 열저장고(heat reservoir) 사이에서 작동하는데, 온도가 높은 고온($ T_H $) 열원으로부터 열( $ q_H $)을 받아 흡수한 열에너지의 일부를 사용하여 피스톤을 움직이는 등의 기계적인 일($ w $)을 외부에 수행하고, 남은 나머지 열에너지 $ q_C $를 저온 열원으로 방출하는 과정을 거치게 된다. 사실 열기관에 대해서는 클라우지우스 및 켈빈-플랑크 서술을 소개했던 포스팅에서 이미 다룬바 있다.
이때, 열기관의 process는 열역학 제 1법칙에 따라 에너지가 보존되어야 한다. 즉, 흡수한 열은 수행한 일과 방출한 열의 합과 같다.
$$ q_H = w + q_L $$
또한 열기관의 성능은 열효율(efficiency $ \eta $)로 평가하고, 투입한 열($ q_H $) 대비 외부에 수행한 일($ W $)의 비율로 정의한다.
$$ \eta = \frac{w}{q_H} = \frac{q_H - q_L}{q_H} = 1 - \frac{ q_L}{q_H}$$
이 식에서 알 수 있듯이, 열효율을 높이려면 고온 열원에서 흡수하는 열 $ q_H $은 최대화하고 저온 열원으로 방출하는 열 $ q_L $은 최소화해야 한다. 만약 이라면 효율 100%를 달성할 수 있겠지만, 이는켈빈-플랑크 서술에 따라 열역학 제2법칙에 위배됨을 이미 살펴본 바 있다.
켈빈-플랑크 서술 (Kelvin-Planck statement)
"열원으로부터 열을 전부 흡수하여 모두 일로 바꾸는 과정은 불가능하다. 즉, 어떤 열기관의 열효율은 100%가 될 수 없다"
2. 카르노 사이클(Carnot Cycle)
그럼 가장 효율적인 열기관은 무엇일까? 그것이 바로 카르노 기관이다. 1824년 프랑스 공학자 사디 카르노(Sadi Carnot)가 제시한 이상적인 열기관으로, 두 열원 사이에서 다음과 같은 네 단계의 가역 과정(reversible process)으로 이루어진 카르노 사이클(Carnot cycle)을 따른다. 아래 그림은 카르노 사이클과 각 단계를 P-V 그래프에 표현한 것이다. 하나씩 살펴보자.

2.1 가역 등온 팽창 (Reversible Isothermal Expansion) : 1 → 2
이상기체가 고온 열원 $T_H$ 과 접촉하여 온도를 일정하게 유지하면서 가역적으로 부피가 $ V_ 1$ 에서 $V_2 $ 으로 팽창하는 과정이다. 이상 기체의 등온 과정에서 내부 에너지 변화 $ dU=C_VdT=0 $이므로, 열역학 제1법칙 $ dU= \delta q−\delta w $에 따라, 계가 흡수한 열 $ q_H$ 은 전부 외부에 한 일 $ w_{1 \to 2} $로 전환된다. 이를 표현하면 아래와 같다.
$$ dU = \delta q - \delta w = 0 \Rightarrow q = w $$
$$ q_H = w_{1\to2} = \int_{V_1}^{V_2} P dV $$
이상 기체 상태 방정식 $ PV=nRT_H $ 를 이용해 압력 P를 부피 V의 함수로 나타내면 다음과 같다.
$$ q_H = \int_{V_1}^{V_2} \frac{nRT_H}{V} dV = nRT_H \ln\left(\frac{V_2}{V_1}\right) $$
이 단계에서 엔트로피 변화도 알아보자. 가역 등온과정에서 엔트로피 변화는 아래와 같이 계산됨을 이미 지난포스팅에서 확인했으므로, 엔트로피 변화는 다음과 같이 주어지겠다.
$$ \Delta S_{1 \to 2} = \int \frac{P}{T} dV = \int \frac{nR}{V} dV = nR \ln{\frac{V_2}{V_1}} $$
2.2 가역 단열 팽창 (Reversible Adiabatic Expansion) : 2 → 3
이상기체가 단열된 상태에서 부피가 $V_2 $에서 $V_3$로 팽창된다. 외부와의 열 교환이 없으므로 $ \delta q = 0 $이고, 열역학 제1법칙 $ dU= \delta q−\delta w $ 에 따라 내부 에너지 감소량이 전부 일로 전환된다. 이로 인해 온도는 $ T_H $ 에서 $ T_L $ 로 떨어지게 된다. 이상기체는 $ dU = C_V dT $, $ \delta w = PdV = \frac{nRT}{V} dV $을 만족하므로 이를 적용하면,
$$ \begin{align}
dU &= \delta q - \delta w = -\delta w \\[10pt]
&\Rightarrow C_V dT = -\frac{nRT}{V} dV\\[10pt]
&\Rightarrow \frac{dT}{T} = -\frac{nR}{C_V} \frac{dV}{V} \\[15pt]
\end{align} $$
가 된다. 위 식을 2 ($T_H , \; V_2 $)에서 3 ($T_L, \; V_3 $) 까지 적분하면, 다음을 얻는다.
$$ \begin{align}
\therefore \int_2^3 \frac{dT}{T} &= -\int_2^3 \frac{nR}{C_V} \frac{dV}{V} \\[10pt]
&\Rightarrow \ln\left( \frac{T_L}{T_H} \right) = -\frac{nR}{C_V} \ln\left( \frac{V_3}{V_2} \right)
\end{align} $$
가역 단열 팽창 단계이므로 $ q $가 0이어서 엔트로피 변화는 $ \Delta S_{2 \to 3} = 0 $ 이다. 자세한 내용은 지난 포스팅을 참고하자.
2.3 가역 등온 압축 (Reversible Isothermal Compression) : 3 → 4
이상기체는 저온 열원 $ T_L $ 과 접촉하여 온도를 일정하게 유지하면서 외부로부터 일을 받아 부피가 $ V_3 $ 에서 $ V_4 $로 가역적으로 압축된다. 가역 등온 팽창 1 → 2 와 마찬가지로 내부 에너지 변화 $ dU=0 $ 이고, 계에 가해진 일 $ w_{3 \to 4} $ 은 모두 열 $ q_L $ 로 방출된다. 따라서 아래와 같이 서술할 수 있다.
$$ \begin{align}
- q_L &= - w_{3\to4} \\[10pt]
&= - \int_{V_3}^{V_4} P dV = - \int_{V_3}^{V_4} \frac{nRT_L}{V} dV \\[10pt]
&= - nRT_L \ln\left(\frac{V_4}{V_3}\right)
\end{align} $$
$ q_L $ 의 부호가 음수이기 때문에, $ - q_L $ 을 방출된 열의 양이라고 보여주기 위해서 위와 같이 표현하였다. 가역 등온 압축 단계이므로, 엔트로피 변화는 2.1 가역 등온 팽창 단계와 비슷하게 다음과 같이 주어질 것이다.
$$ \Delta S_{3 \to 4} = nR \ln{\frac{V_4}{V_3}} $$
2.4 가역 단열 압축 (Reversible Adiabatic Compression) : 4 → 1
다시 이상기체를 단열시킨 상태에서 부피가 $ V_4 $ 에서 $ V_1 $ 으로 압축되어 처음 상태로 돌아가게 된다. 외부에서 가해진 일은 기체의 내부 에너지로 전환되어, 온도는 $ T_L $ 에서 $ T_H $ 로 상승하게 된다. 가역 단열 팽창 2 → 3 과 마찬가지로,
$$ \frac{dT}{T} = -\frac{nR}{C_V} \frac{dV}{V} $$
을 따르게 되고, 이 식을 4 ($T_L , \; V_4 $)에서 1 ($T_H, \; V_1 $) 까지 적분하면, 다음을 얻는다.
$$ \begin{align}
\therefore \int_4^1 \frac{dT}{T} &= -\int_4^1 \frac{nR}{C_V} \frac{dV}{V} \\[10pt]
&\Rightarrow \ln\left( \frac{T_H}{T_L} \right) = -\frac{nR}{C_V} \ln\left( \frac{V_1}{V_4} \right)
\end{align} $$
가역 단열 팽창 단계이므로 2.2 가역 단열 팽창과 똑같이, 엔트로피 변화는 $ \Delta S_{4 \to 1} = 0 $ 이다.
2.5 엔트로피 변화
카르노 사이클에서 엔트로피 변화를 계산해보자. 2.2/2.4의 가역 단열 팽창/압축 단계에서는 엔트로피 변화 $ \Delta S = 0 $ 이었음을 확인하였다. 따라서 전체 사이클의 엔트로피 변화는 2.1 가역 등온 팽창 단계와 2.3 가역 등온 압축 단계에서의 엔트로피 변화 합과 같다.
$$ \begin{align} \Delta S &= \Delta S_{1 \to 2} + \Delta S_{3 \to 4} \\[10pt] & = nR \ln{\frac{V_2}{V_1}} + nR \ln{\frac{V_4}{V_3}} =nR \ln{\frac{V_2 V_4}{V_1 V_3}} \end{align} $$
여기서, 가역 단열 팽창/압축 단계의 계산 결과를 살펴보자.
$$ \ln\left( \frac{T_L}{T_H} \right) = -\frac{nR}{C_V} \ln\left( \frac{V_3}{V_2} \right) \;\; , \;\; \ln\left( \frac{T_H}{T_L} \right) = -\frac{nR}{C_V} \ln\left( \frac{V_1}{V_4} \right) $$
이므로, 위 두 식을 더하면 다음의 결과를 얻는다.
$$ \begin{align} \ln\left( \frac{T_L}{T_H} \right) + \ln\left( \frac{T_H}{T_L} \right) &= -\frac{nR}{C_V} \ln\left( \frac{V_3}{V_2} \right) -\frac{nR}{C_V} \ln\left( \frac{V_1}{V_4} \right) \\[10pt] &= -\frac{nR}{C_V} \ln\left( \frac{V_1 V_3}{V_2 V_4 } \right) = 0 \\[10pt] \Rightarrow & V_1 V_3 = V_2 V_4 \end{align} $$
이 식을 엔트로피 변화 $ \Delta S $ 식에 대입해보자. 그러면, 엔트로피 변화 $ \Delta S = 0 $ 이라는 결과를 얻을 수 있다.
$$ \Delta S = nR \ln{\frac{V_2 V_4}{V_1 V_3}} = 0 $$
따라서, 카르노 사이클의 엔트로피 변화는 0 이라는 사실을 얻을 수 있다. 사실 엔트로피는 상태함수이기 때문에 당연한 결과라고 할 수 있지만, 밑의 4번에서 왜 엔트로피가 상태함수인지 증명하기 위해서 이 결과를 사용하게 될 것이다.
2.6 카르노 기관의 효율 (Efficiency of Carnot Cycle)
카르노 사이클은 위와 같이 네 단계를 거친다는 것을 살펴보았다. 이때, 카르노 기관의 열효율(efficiency $ \eta $)을 계산해보자. 열효율은 1.에서 언급한대로, 공급된 열($ q_H $) 대비 외부에 한 일($ W $)의 비율로 정의한다. 위에서 계산한 가역 등온 팽창 시 계가 흡수한 열 $ q_H $ 와 가역 등온 압축 시 방출된 열 $ q_L $을 이용해서 열효율을 계산할 수 있다.
$$ \begin{align}
\eta &= \frac{q_H - (-q_L)}{q_H} = \frac{nRT_H \ln\left( \frac{V_2}{V_1} \right) - nRT_L \ln\left( \frac{V_3}{V_4} \right)}{nRT_H \ln\left( \frac{V_2}{V_1} \right)} \\[10pt]
&= 1 - \frac{T_L}{T_H}
\end{align} $$
$ V_1 V_3 = V_2 V_4 $ 임을 사용하여 정리하면, 열효율이 $ \eta =1 - \frac{T_L}{T_H} $라는 놀랍고도 단순한 결과를 얻게 된다.
3. 열역학 제 2법칙 (카르노 기관)
지금까지 카르노 기관의 순환 과정과 열효율을 살펴보았는데, 이게 열역학 제 2법칙과 어떤 관련이 있는지 알아보자.
카르노 정리(Carnot's theorem)
카르노 정리는 어떤 온도가 다른 두 열원 사이에서 작동하는 모든 "가역적 열기관"의 열효율은 모두 동일하고, 두 열원 사이에서 작동하는 모든 열기관은 가역적 열기관의 열효율보다 높을 수 없다는 정리다. 볼드체의 두 문장이 중요하다. 이 둘의 증명은 각각 귀류법을 이용해서 간단하게 증명할 수 있다. 과정이 궁금하다면, 위키피디아 Carnot's theorem (thermodynamics) 문서를 참고하자.
카르노 기관은 네 가지의 가역적 단계로 구성되어 있으므로 가역적 열기관이고, 만들 수 있는 수많은 가역적 열기관 중 하나일 뿐이다. 즉, 카르노 사이클과는 다른 어떤 가역적 사이클을 구성하더라도, 열효율은 위에서 계산한 카르노 기관의 열기관의 열효율과 똑같다는 말이다. 수많은 가역적 사이클 중, 카르노 기관이 가장 대표적이기 때문에 열역학에서 자주 다뤄지는 것이라고 생각하면 되겠다. 위에서 계산한 카르노 기관의 열효율은 달성할 수 있는 열효율의 최대 상한이라는 말이다.
이러한 사실을 정리하면 다음과 같은 서술로 정리할 수 있는데, 이는 열역학 제 2법칙의 하나의 서술이 된다.
모든 가역적 열기관의 열효율은 모두 동일하고, 두 열원 사이의 온도에만 종속되며, 어떠한 열기관도 가역적 열기관의 열효율(카르노 기관의 열효율)을 뛰어넘을 수 없다. 카르노 기관은 가역적 열기관의 한 종류이다.
4. 엔트로피와 카르노 사이클
카르노 사이클로부터 엔트로피가 상태함수임을 확인해보자. 2.6 카르노 기관의 열효율 계산으로부터 우리는, 다음의 결과를 도출할 수 있다.
$$ \eta = \frac{q_H - (-q_L)}{q_H} = 1 - \frac{T_L}{T_H} $$
$$ \therefore \frac{q_H}{T_H} + \frac{q_L}{T_L} = 0 $$
위의 식은 카르노 사이클의 엔트로피 변화량이 $ \Delta S = 0 $ 라는 사실과 같은 결과이다. 아래 그림과 같이 어떤 폐순환 경로가 있다고 가정하자. 이 경로는 아래 그림처럼 무한히 작고 무수히 많은 카르노 사이클들의 합과 같다고 할 수 있다.
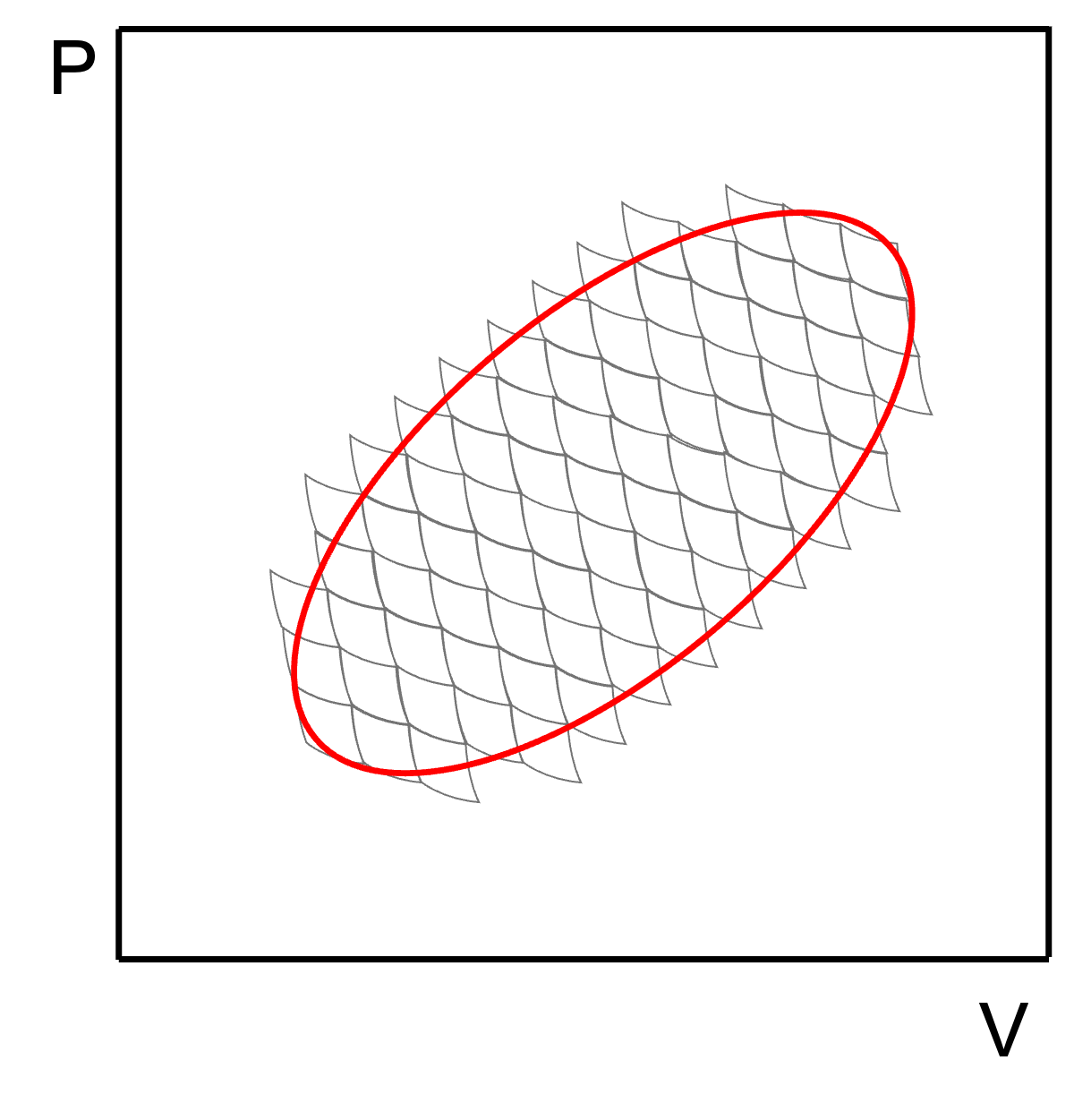
따라서, 각 카르노 사이클의 $ \frac{q}{T} $ 의 합은 결과적으로 전체 경로를 따라 적분한 결과와 같다. 이를 수식적으로 표현하면 다음과 같다.
$$ \sum_{\text{all}} \frac{q}{T} = 0 \leftrightarrow \oint \frac{\delta q}{T} = 0 $$
새로운 열역학적 양(thermodynamic quantity) $ S $ 를 다음과 같이 정의한다면,
$$ dS = \frac{\delta q}{T} $$
S는 아래와 같이 폐곡선에 대한 적분값이 0이므로, (즉, 위의 경로를 따라 한 바퀴를 S에 대해 적분한 값이 0이므로)
$$ \oint dS = 0 $$
S는 상태함수(State function)가 된다. 이렇게 카르노 사이클로부터 엔트로피가 상태함수라는 사실을 유도할 수 있다.
오늘 포스팅까지, Chapter 1 열역학의 기본 개념과 열역학 법칙을 다뤄보았다. 계와 주위의 정의부터 시작해서, 여러 열역학적 양들을 정의하고, 이들을 이용하여 열역학 제 1법칙과 2법칙, 여러 중요 개념들을 표현해보았다. 열역학을 공부함에 있어서 가장 기본이 되는 내용들인 만큼 꼭 알아두었으면 한다. 최대한 자세하게 서술해보려고 노력했으니, 천천히 읽어보면 많은 도움이 될 것 같다는 생각이 든다.
다음 포스팅부터는 Chapter 2 열역학 퍼텐셜(Thermodynamic Potentials)에 대해 다뤄보려 한다.
궁금한 내용이나 질문이 있다면 댓글로 달아주면 친절히 답변할 수 있도록 하겠고, 그럼 다음 포스팅에서 만나요~!! 안녕~~!!




