[열역학] 1.6 열역학 제 2법칙 - 정의, 클라우지우스 서술과 켈빈-플랑크 서술, 열역학 제 1법칙과의 결합

지난 포스팅에서는 열역학적인 자발과 비가역성에 대해 그 의미를 알아보고, 이와 관련된 클라우지우스 부등식, 열역학 제 2법칙과 엔트로피의 정의에 대해 알아보았다. 사실, 지난 포스팅에서 다룬 열역학 제 2법칙은 엔트로피의 정의를 이용하여 수식적으로 서술한 것이고, 이외에도 여러 다양한 서술(Statement)들이 존재한다. 오늘은 그 중, "클라우지우스의 서술(Clausius statement)"과 " 켈빈-플랑크(Kelvin-Planck statement)"을 다뤄보고, 두 서술의 동등성을 살펴보겠다.
뿐만 아니라, 앞서 살펴본 열역학 제 1법칙과 열역학 제 2법칙은 어떤 관련이 있는지, 두 법칙은 어떻게 결합될 수 있는지도 함께 살펴보도록 하겠다.
결론적으로, 열역학 제 2법칙의 본질을 더 쉽게 이해할 수 있도록 설명해보려 한다. 차분하게 한 줄씩 읽어보기를 권장한다.
이 글을 읽기 전에 앞선 포스팅을 참고하면, 이해하는데 도움이 될 것 같다.
[열역학] 1.5 자발, 비가역성과 엔트로피, 클라우지우스 부등식-(Spontaneous, Irreversibility and Entropy, In
[열역학] 1.5 자발적 과정과 비가역적 과정, 비가역성과 엔트로피, 클라우지우스 부등식-Spontaneous and Irreversible Process, Irreversibility and Entropy, Inequality of Clausius 지난 포스팅까지는 열역학 제 1법칙에
gyuuuul.tistory.com
그럼 시작해보자~~!!
1. 열역학 제 2법칙(Second law of thermodynamics)
앞선 포스팅에서는 비가역적 과정, 클라우지우스 부등식을 이용하면 열역학 제 2법칙을 수학적으로 표현하는 방법을 알아보았다. 그리고 열역학 제 2법칙에는 다양한 서술들이 있는데, 다음 서술의 의미를 이해해보았다. (여기 앞선 포스팅을 참고해보자.)
"자연계에서의 모든 자발적 과정은 엔트로피를 증가시키는 방향으로 진행된다"
좁게는, "고립계의 엔트로피는 감소하지 않는다."
고립계에서는 출입하는 열( $ \delta q = 0 $ )이 없으므로, 클라우지우스 부등식을 적용하면 다음이 성립한다.
$$ dS \geq \frac{\delta q}{T} = 0 $$
$$ dS \geq 0 $$
따라서, 고립계에서 엔트로피는 절대로 감소하지 않는다는 사실을 확인하였고, 등호는 가역적 과정일 때 $ dS = 0 $ 이 성립한다. 비가역적 과정에서 엔트로피는 언제나 증가하게되었다. ( $ dS > 0 $ ) 우주를 하나의 계라고 생각하면 열출입이 없으므로 고립계라고 볼 수 있고, 따라서 모든 자연계의 자발적 과정은 우주의 엔트로피를 증가시키는 방향으로 진행한다는 말과 동치가 됨을 확인해보았다.
사실 열역학 제 2 법칙은 다양한 방식으로 서술될 수 있는데, 그 중 대표적인 표현은 다음 두가지가 있다.
1. 클라우지우스의 서술(Clausius statement)
"열은 주위에 어떠한 변화를 발생하지 않으면서 저온의 물체에서 고온의 물체로 전달될 수 없다."
2. 켈빈-플랑크(Kelvin-Planck statement)
"열원으로부터 열을 전부 흡수하여 모두 일로 바꾸는 과정은 불가능하다. 즉, 어떤 열기관의 열효율은 100%가 될 수 없다"
오늘 포스팅에서는 이 두 서술에 대해서 자세히 살펴보고, 열역학 제 2법칙의 다양한 서술들이 모두 동치임을 확인해보도록 하자.
2. 클라우지우스 서술과 켈빈-플랑크 서술의 동등성(Equivalence of the Clausius and the Kelvin statements)
1번에서 언급한 "클라우지우스의 서술"과 "켈빈-플랑크 서술"은 동등한 결과를 나타내게 된다. 언뜻 보기에는 전혀 다른 말인 것 같지만, 차근차근 하나씩 의미를 곱씹어가면서 알아가보자.
아래 그림과 같이 켈빈-플랑크 서술을 위반하는 열기관을 생각해보자. 즉, Hot Reservoir(뜨거운 열원)으로부터 흡수한 열 $ Q_H $을, 주위와 어떠한 상호작용 없이 100% 일($ W $)로 전환할 수 있는 열기관이 존재한다고 생각해보자.

이 켈빈-플랑크 서술을 위반하는 열기관 옆에 어떤 냉장고(refrigerator)를 달아서, 두 열기관을 결합했다고 생각하자. (이 냉장고는 실제 열기관이므로, 냉장고의 효율은 카르노 열기관의 효율을 넘길 수 없다. 카르노기관에 대해서는 다음 포스팅에서 설명하겠다.) 그렇게 되면, 결론적으로 결합된 열기관은 Cold Reservoir에서 $ Q_L $의 열을 받아, 열기관(Heat Engine)으로 받은 $ Q_H $을 제외하고, 순전히 $ Q_L $의 열을 Hot Reservoir로 전달하게 된다. 따라서 이 열기관은 저온에서 고온으로, 외부의 영향을 받지 않고, 열을 이동시키는 열기관이 되는 것이다.

이는 클라우지우스 서술을 위반한다.
이번에는 반대로, 아래 그림과 같이 클라우지우스 서술을 위반하는 열기관을 생각해보자. 즉, 주위로부터 어떠한 영향을 받지 않고 저온에서 고온으로 열을 전달시키는 기관(냉장고: Refrigerator)이 존재한다고 생각하자.
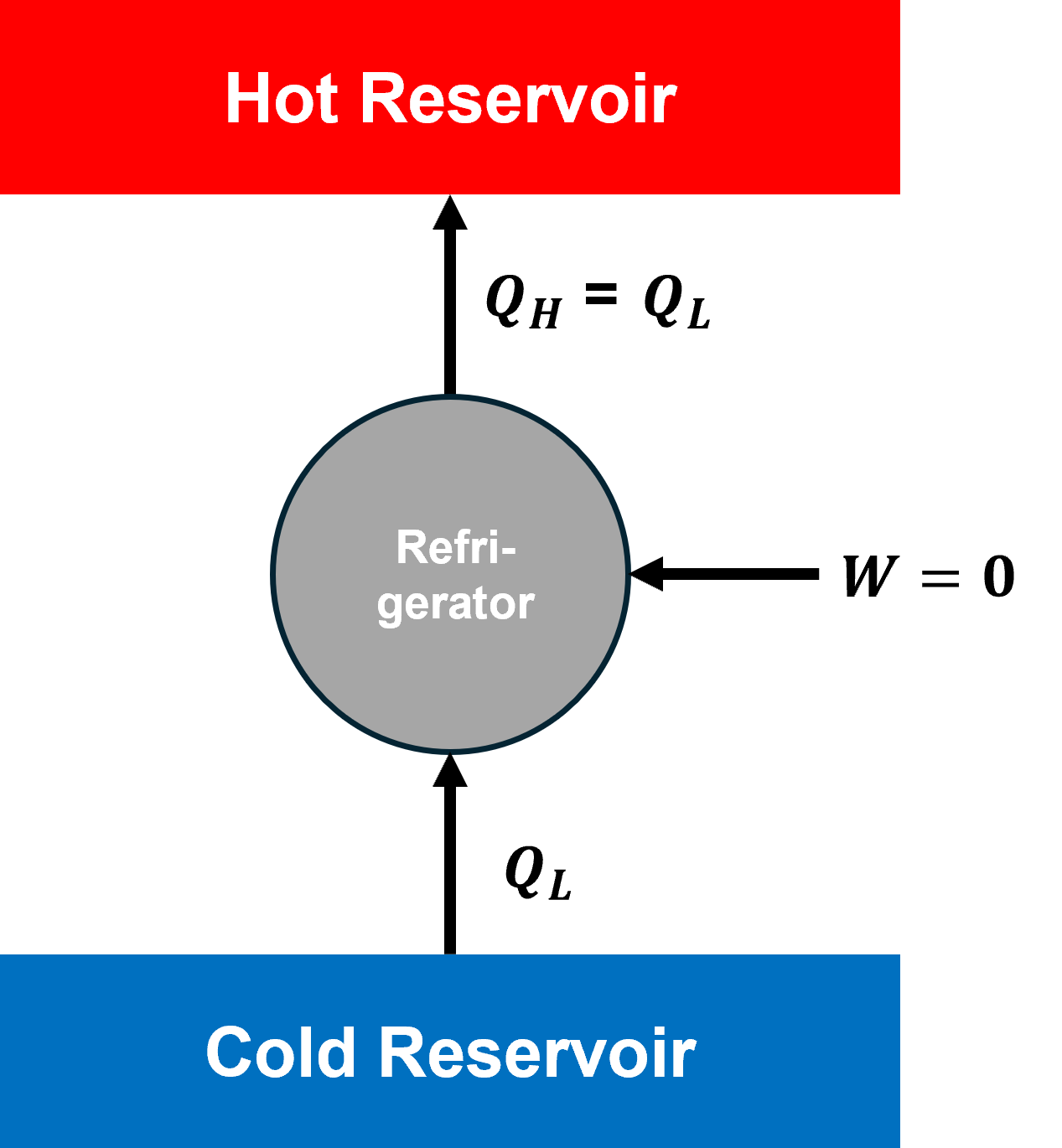
이 클라우지우스 서술을 위반하는 열기관 옆에 어떤 열기관(Heat engine)을 달아서, 위와 마찬가지로 두 기관을 결합하자.(마찬가지로 이 열기관도 실제 열기관이므로, 열효율은 카르노 열기관의 열효율을 넘길 수 없다) 그러면, 결론적으로 결합된 열기관은 Hot Reservoir에서 $ Q_H - Q_L $의 열을 받아서 모두 일 $ W $로 바꿀 수 있게 된다. 따라서, 이 열기관은 열원으로부터 열을 전부 흡수하여 모두 일로 바꿔주는 열기관이 된다.

이는 켈빈-플랑크 서술 위반이 된다.
따라서, 클라우지우스 서술과 켈빈-플랑크 서술, 둘 중 하나를 위반하는 열기관은 반드시 다른 하나의 서술을 위반하게 되므로, 두 서술은 동등하다는 사실을 알 수 있다.
3. 열역학 1법칙과 2법칙의 결합
두 포스팅에 걸쳐서, 자발, 비가역성, 엔트로피, 열역학 제2법칙에 대해서 다뤄보았다. 열역학 제 2법칙은 위에서와 같이, "고립계의 엔트로피는 감소하지 않는다.", " 모든 자연계의 자발적 과정은 우주의 엔트로피를 증가시키는 방향으로 진행한다."는 말로 서술할 수 있다. 수식적으로는 클라우지우스 부등식을 이용해 아래와 같이 정리할 수 있었다.
$ dS \geq \frac{\delta q}{T} = 0 $
$ dS \geq 0 $
이때, 엔트로피는 앞선 포스팅에서 다음과 같이 정의하였다.
$$ dS = \frac{\delta q_{rev}}{T} \;\;\; S = \int \frac{\delta q_{rev}}{T} $$
또한, 앞선 포스팅에서 다루었듯, 열역학 제 1법칙으로부터 다음의 결과를 알고 있다.
$$ dU = \delta q - \delta w $$
엔트로피의 정의로부터 $ \delta q_{rev} = TdS $ 임을 얻었으므로, 가역과정일 경우에 위 식에 대입하면 다음의 관계식을 얻을 수 있다.
$$ dU= TdS - PdV $$
즉, 내부에너지 $ U $를 엔트로피 $ S $와 부피 $ V $의 함수 $ U=U(S, V) $ 로 표현할 수 있다는 뜻이다. 이렇게 열역학 제 1법칙과 제 2법칙을 결합하여 매우매우 중요한 관계식을 유도할 수 있다. (열역학에서 가장 중요한 식이지 않나 싶다)
내부에너지는 상태함수(State Function)이므로, 다음과 같은 전미분의 형식을 취할 수 있다. (사실 상태함수는 exact하다. 이 성질은 Maxwell relation에서 자세히 다뤄보도록 하겠다.)
$$ dU = \frac{\partial U}{\partial S} \Bigr |_V dS + \frac{\partial U}{\partial V} \Bigr |_{S} dV $$
위의 결합식과 비교하면, 온도와 압력을 다음과 같이 정의할 수 있게 된다.
$$ T = \frac{\partial U}{\partial S} \Big |_V $$
$$ P = - \frac{\partial U}{\partial V} \Big |_S $$
오늘 포스팅에서는 지난 포스팅에 이어서 열역학 제 2법칙의 다양한 서술 중 클라우지우스의 서술과 켈빈-플랑크의 서술, 두 서술의 동등성에 살펴보았고, 열역학 제 1법칙과 2 법칙의 결합을 통해 매우 중요한 관계식을 유도해보았다.
사실 열역학 제 2법칙의 서술들 중에서 중요한 표현 중에 하나가 더 있는데, 바로 "카르노 기관"과 관련된 것이다. 이 부분은 다음 포스팅에서 자세하게 다뤄보도록 하겠다.
궁금한 내용이나 질문이 있다면 댓글로 달아주면 친절히 답변해보도록 하겠다.
그럼 다음 포스팅에서 만나요~!! 안녕~~!!

'전공 공부정리 > 열역학' 카테고리의 다른 글
| [열역학] 1.8 카르노 기관 (0) | 2025.09.17 |
|---|---|
| [열역학] 1.7 열역학 제 2법칙 - 등온과정, 단열과정, 자유팽창 (0) | 2025.09.17 |
| [열역학] 1.5 자발, 비가역성과 엔트로피, 클라우지우스 부등식-(Spontaneous, Irreversibility and Entropy, Inequality of Clausius) (0) | 2025.06.22 |
| [열역학] 1.4 열용량(Heat Capacity) (1) | 2025.06.20 |
| [열역학] 1.3 열역학 제 1법칙 - 등온과정, 단열과정 (0) | 2025.06.20 |



